Produkty wietrzenia chemicznego (jony Ca2+ i HCO3–) powstały ze skał węglanowych (CaCO3) w reakcji chemicznej z absorbowanym z atmosfery dwutlenkiem węgla (CO2) i wodą (H2O) pochodzącą z wód gruntowych lub pobliskich rzek, w których z kolei powstają wspomniane zarówno jony wapnia Ca2+ (kationy), jak i jony wodorowęglanu HCO3– (aniony).
CaCO3 (s) + CO2 (g) + 2H2O (l) -> Ca2+ (aq) + 2 HCO3– (aq)
Gdy reakcje chemiczne przebiegają bez zakłóceń i nie brakuje jonów wapnia, to wody są w miarę umiarkowanie uzasadowione wokół pH grubo powyżej 8,1, choć w coraz większej liczbie tropikalnych wód oceanicznych zakwaszenie postępuje i pH obniżyło się tam już do granicy 8,1 pH. Zwłaszcza tak się stało wokół Wielkiej Rafy Koralowej u wybrzeży północno-wschodniej Australii (Lee Kump i in., 2009). Ogólnie na całej Ziemi, ocieplenie wpływa na to, że coraz mniej powstaje jonów wapnia i wodorowęglanów, z których powstają potem budulcowe aniony węglanowe, jako produktów wietrzenia chemicznego. Ponadto dwutlenek węgla coraz gorzej rozpuszcza się w tropikalnej wodzie oceanicznej, która staje się coraz cieplejsza, a przez to również coraz kwaśniejsza, gdyż to są przyczyny, że rośnie nadmiar nierozpuszczonego CO2 w wodzie oceanicznej. Podczas rozpuszczania dwutlenku węgla powinna powstać następująca reakcja chemiczna, w której po rozpuszczeniu dwutlenku węgla w reakcji z wodą powstaje kwas węglowy (Ove Hoegh-Guldberg i in., 2007), który następnie w chłodnej wodzie łatwo dysocjuje tworząc po kolei aniony wodorowęglanowe HCO3– i aniony węglanowe CO32- oraz kationy wodorowe H+.
CO2 + H2O -> H2CO3 -> HCO3– + H+ -> CO32- + H+
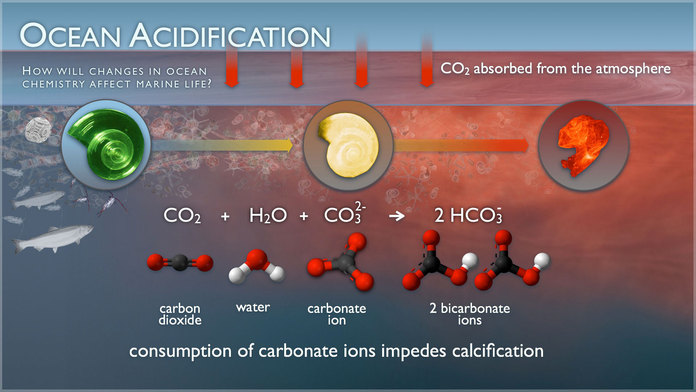
Rysunek. Konsumpcja jonów węglanowych (anionów CO32-) hamuje kalcyfikację (powstanie węglanu wapnia CaCO3). Nie dopuszcza do fuzji z nimi jonów wapnia (kationów Ca2+). (NOAA)
Aniony węglanowe CO32- w ocieplonej i zakwaszonej wodzie wchodzą w reakcję z dwutlenkiem węgla i z wodą. Tworzą wówczas następującą reakcję (tak jak na rysunku powyżej):
CO2 + H2O + CO32- -> 2HCO3–
Powstają dwa jony wodorowęglanu. I to jest główny czynnik zakwaszenia oceanów. Podwojona produkcja kwaśnych związków chemicznych, których obecnie w tropikalnych wodach, gdzie występują rafy koralowe, jest bardzo dużo.
W nieodległej przeszłości, jeszcze w XIX wieku, w nieocieplonej i niezakwaszonej wodzie, aniony CO32- w fuzji z kationami wapnia Ca2+ tworzą węglan wapnia. Składnik budulcowy muszli i skorupek u bezkręgowców.
Ca2+ + CO32- -> CaCO3
Dwutlenek węgla nierozpuszczony reagując z wodą zmienia się w coraz powszechniejszy w oceanach kwas węglowy H2CO3, który z kolei wtedy coraz rzadziej dysocjuje na kationy wodorowe H+ i dobrze nam znany anion wodorowęglanowy HCO3– i budulcowy anion węglanowy CO32-. Niestety w oceanach coraz mniej jest też kationów wapnia Ca2+, budujących muszle i skorupki u bezkręgowców. Zarówno ocieplenie, jak i zakwaszenie wpływają na to, że pH oceanów drastycznie spada, a to oznacza totalne spustoszenie flor i faun zamieszkujących największe akweny świata.
Niestety ludzie dalej ignorują ten poważny problem. Ignorują nawet coś co powinno im przynieść wymierne korzyści gospodarcze. Postępujące ocieplanie i zakwaszanie wód oceanicznych przyczynia się już do spadku rybołówstwa w wielu regionach Ziemi. Niedługo w ogóle w oceanach świata zabraknie ryb i wszelkiego rodzaju „owoców morza”, w postaci krewetek, langust, krabów, homarów, małży. Do tej katastrofy doprowadzamy sami poprzez beztroskie spalanie paliw kopalnych i wylesianie Ziemi (James Orr i in., 2005).
https://www.pmel.noaa.gov/co2/story/Ocean+Acidification
https://theotherco2problem.wordpress.com/what-happens-chemically/
http://www.lenntech.com/periodic/water/calcium/calcium-and-water.htm
