W drugiej połowie XVIII wieku miało swój początek pierwsze spalanie paliw kopalnych, a konkretniej emisje dwutlenku węgla. I to nie tylko do atmosfery, ale i też, z większym upływem czasu, do oceanów. Z tą jednak różnicą, że rosnące stężenie dwutlenku węgla w wodach oceanicznych nie przyczynia się do zatrzymywania energii cieplnej w zakresie w podczerwieni, jak to się dzieje właśnie w atmosferze, ale powoduje inną zmianę klimatu – zakwaszenie oceanów.
Cząsteczka dwutlenku węgla, reagując z cząsteczką wody, zamienia się się w słaby kwas węglowy, który ulega dysocjacji na jony: aniony wodorowęglanowe i kationy wodorowe, i następnie, na aniony węglanowe i znowu na kationy wodorowe.
CO2 + H2O > H2CO3 ; H2CO3 > HCO3– +H+ ; HCO3– > CO32- + H+
–
Gdy rośnie stosunek anionów wodorowęglanowych względem węglanowych, robi się problem
W obiegu węglowym atmosferyczny dwutlenek węgla jest cały czas w interakcji z oceanami. Problem jednak zaczyna się robić, gdy tego najważniejszego gazu w systemie klimatycznym, pojawia się znacznie więcej niż potrzeba. To znaczy, gdy rośnie stosunek anionów wodorowęglanowych względem węglanowych i gdy zaczyna tych drugich brakować do budowy skorupek u skorupiaków i muszli u małży.
Oceany, tak jak i lądy, mniej więcej w naturalnych procesach tyle samo emitują co absorbują dwutlenku węgla. Jednak od uruchomienia pierwszych manufaktur opalających węgiel w Wielkiej Brytanii, również stężenie tego gazu zaczęło powoli wzrastać w oceanach, a temperatura i energia cieplna w największych akwenach wodnych Ziemi zaczęła rosnąć dopiero od lat 70 XX wieku, gdy unowocześniono pomiary i zaobserwowano na wykresach szybki wzrost tych parametrów.
Jak czytamy w pracy naukowej, opublikowanej, w instytucji naukowej NOAA – Morskim Laboratorium Środowiska Pacyficznego (PMEL – Pacific Marine Environment Laboratory), przez badaczy zakwaszenia oceanów: Richarda Feely’ego, Christophera Sabine i Victorię Fabry, od początku ery przemysłowej ocean wchłonął z atmosfery około 525 miliardów ton CO2 1.
A więc w 2006 roku było to już około 22 milionów ton dziennie.
Autorzy serwisu Smithsonian Institution piszą tak 2:
Początkowo naukowcy myśleli, że może to być dobre rozwiązanie, ponieważ pozostawia mniej dwutlenku węgla w powietrzu, aby ogrzać planetę. Ale w ostatniej dekadzie zdali sobie sprawę, że to spowolnione ocieplenie odbywa się kosztem zmiany chemii oceanu. Kiedy dwutlenek węgla rozpuszcza się w wodzie morskiej, woda staje się bardziej kwaśna, a stężenie (pH) oceanu (miara kwasowości lub zasadowości oceanu) spada. Chociaż ocean jest ogromny, wystarczająca ilość dwutlenku węgla może mieć duży wpływ. Tylko w ciągu ostatnich 200 lat woda w oceanie stała się o 30 procent bardziej kwaśna – szybciej niż jakakolwiek znana zmiana chemiczna oceanu w ciągu ostatnich 50 milionów lat.
–
Eksperyment z mezokosmami: badanie organizmów morskich w stosunku do poziomu zakwaszenia
Jeden z najważniejszych eksperymentów badania wpływu zakwaszenia oceanu na gatunki oceaniczne i morskie – Mesocosm – został przeprowadzony w pelagialu u wybrzeży Norwegii w 2015 r. Projektem tym kierował Ulf Riebesell, profesor Biologicznej Oceanografii, pracujący w GEOMAR – Centrum Badań Oceanicznych im. Helmholtza w Kilonii 3.
Badania przeprowadzone zostały w ośmiu mezokosmach o pojemności 55 000 litrów każdy. Są to eksperymentalne zbiorniki wodne umieszczone w morzu lub w oceanie i obsługiwane przez 36 badaczy, którzy przez 50 dni pobierali próbki.
Projekt ten pokazał, że kluczowe gatunki w skali globalnej o strukturze wapiennej jak glon Emiliania huxleyi czy zwierzę bezkręgowe – mięczak, pteropod, czyli morski ślimak skrzydłonogi Limacina helicina, będą głównymi przegranymi.
Wspomniany glon Emiliania huxleyi odgrywa dwie ważne role klimatyczne. Po pierwsze, transportuje węgiel w głębiny oceaniczne opadając po śmierci, a więc, łagodzi klimat. Po drugie, wytwarza chłodny i jasny gaz aerozolowy – dimetylek siarczku (DMS – Dimethyl Sulfoxide), dzięki czemu chmury bieleją, głównie stratocumulusy nad oceanami, i silnie odbijają w przestrzeń kosmiczną promienie słoneczne. A więc, w tym przypadku ten glon ochładza klimat. Z kolei ślimak skrzydłonogi Limacina helicina jest bardzo ważnym ogniwem w sieci troficznej, służącym jako pokarm dla wielu ryb i morskich ssaków (zwłaszcza waleni) i ptaków. Gdy go zabraknie w ekosystemie pelagicznego planktonu, to łańcuchy i sieci pokarmowe po prostu załamią się i może dojść do katastrofy ekologicznej. Mięczak ten jest uzależniony od wysokiego nasycenia wód pelagicznych aragonitem.
–

Fot.1. Skaningowa mikrografia elektronowa pojedynczej komórki Emiliania huxleyi (z witryny internetowej).

Fot.2. Żywy osobnik Limacina helicina (z witryny internetowej).
–
Do zwycięzców należą gatunki niewapienne – pikoplanktonowe, jak bakterie, a wśród bezkręgowych zwierząt, megaplanktonowe osłonice Oicopleura doica, a także z pewnością wiele innych o galaretowatym kształcie zwierząt, jak inne gatunki osłonic czy też wiele gatunków meduz.
—

Fot.3.: po lewej: Studium lokalizacji eksperymentów KOSMOS. po prawej: mezokosmosy KOSMOS rozmieszczone u wybrzeży Ny Ålesund na Svalbardzie. Źródło: Signe Klavsen – GEOMAR/CC BY 4.0.

Fot.4. Trzy z dziesięciu mezokosmów Kilonia KOSMOS w Gullmar Fjord w Szwecji. Źródło: Maike Nicolai – GEOMAR/CC BY 4.0.
–
Organizmy morskie są wystawione na promieniowanie fotosyntetycznie aktywne
Kunshan Gao, z Państwowego Kluczowego Laboratorium Nauk o Środowisku Morskim i Wyższej Szkoły Nauk o Oceanie i Ziemi na Uniwersytecie w Xiamen w Chinach, wraz ze swoim zespołem badawczym, zaobserwował, że wzrost stężenia atmosferycznego dwutlenku węgla wynosi obecnie 0,5% rocznie. I właśnie ono przyczynia się do zakwaszenia oceanu (OA – Ocean Acidification).
Gdy powierzchniowe górne warstwy wody nie mieszają się (UML – upper mixed layer), to gatunki morskie, zwłaszcza fotosyntetyczne glony, są bardziej narażone na zwiększoną dzienną ekspozycję dawki promieniowania fotosyntetycznie aktywnego (PAR Photosynthetically Active Radiation) i promieniowania ultrafioletowego (UV – Ultraviolet). Stratyfikacja oceanu sprzyja również zmniejszonym dostawom składników pokarmowych z dna i głębin oceanicznych oraz zmniejszonemu rozpuszczaniu się tlenu i tworzeniu się stref beztlenowych, co stanowi już dziś bardzo poważne zagrożenie dla flory i fauny w wielu akwenach oceanicznych morskich. 4
—
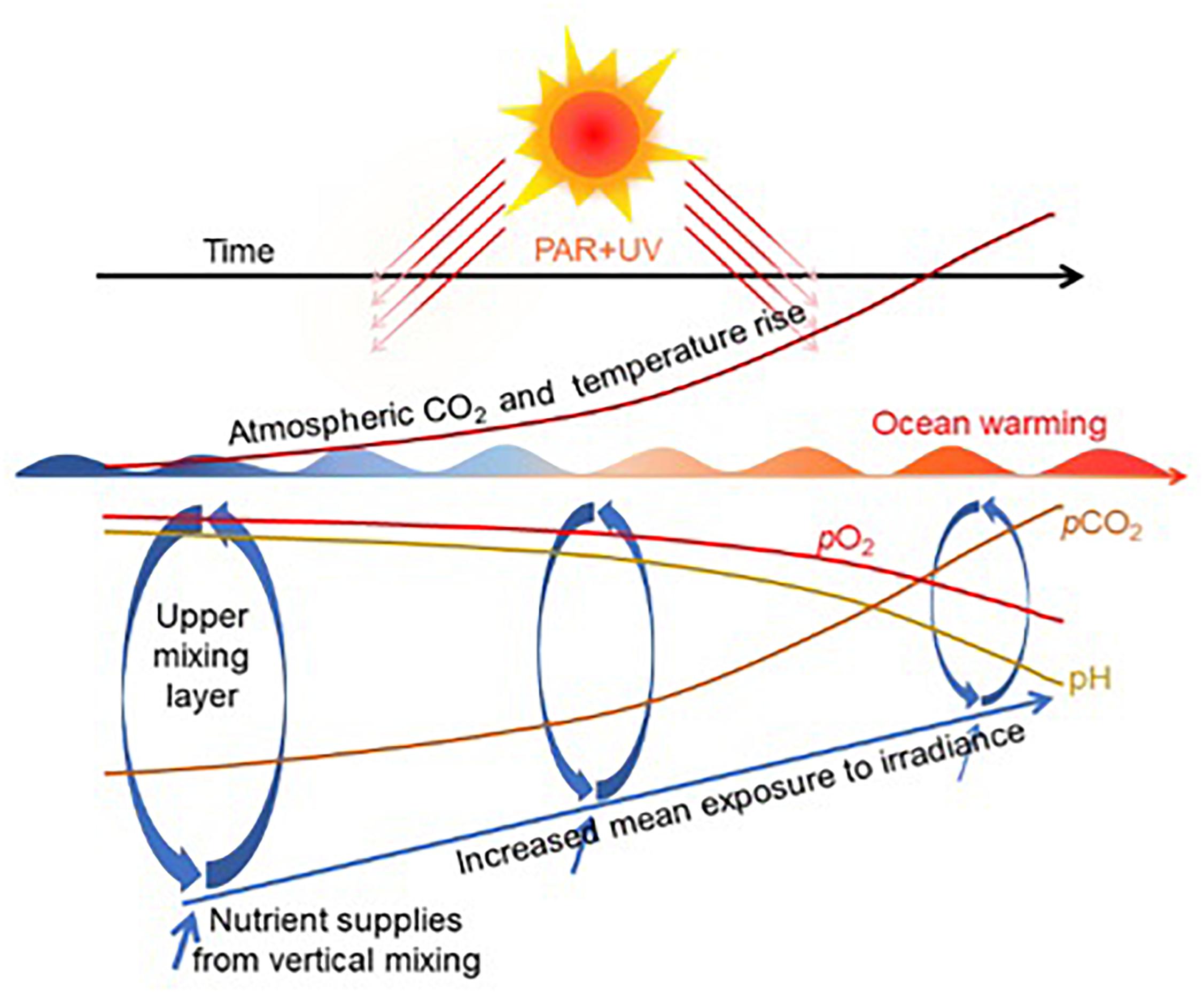
Rys.1. Zakwaszenie oceanu, ocieplenie i odtlenienie związane z rosnącym wzrostem CO2 w atmosferze . Zaleganie górnej warstwy mieszanej (UML) w wyniku ocieplenia naraża żyjące tam organizmy na wyższe poziomy promieniowania słonecznego [Źródło: przerysowano na podstawie Kunshan Gao et al., 2012a/CC BY 4.0) oraz David Hutchins & Feixue Fu, 2017/CC BY 4.0.
—
Autorzy w swojej pracy napisali:
Oceany pobierają ponad 1 milion ton antropogenicznego CO2 na godzinę, zwiększając poziom ciśnienia parcjalnego rozpuszczonego dwutlenku węgla (pCO2) i obniżając stężenie (pH) wody morskiej w procesie zwanym zakwaszeniem oceanów (OA – Ocean Acidification).
–
Zakwaszenie oceanu przyczynia się do spadku poziomu tlenu w wodzie
Ze wszystkich organizmów fotosyntetyzujących na Ziemi, morskie organizmy odpowiadają za około połowę globalnego wiązania węgla (Paul Falkowski & John Raven, 2013). W większości oceanów dominującymi fotoautotrofami są gatunki fitoplanktonowe: jednokomórkowe mikroglony i sinice, których habitaty występują przede wszystkim na otwartych wodach oceanów. Natomiast duże glony, makroglony, oraz trawy morskie preferują głównie siedliska przybrzeżne. Na te organizmy wpływa zarówno wzrost ciśnienia parcjalnego dwutlenku węgla (pCO2) , jak i spadek stężenia wód (pH) wraz z trwającym zakwaszeniem oceanu (OA – Ocean Acidification).
Ocieplenie oceanu prowadzi do spadku rozpuszczalności tlenu w górnej warstwie oceanu, a to oznacza jego odtlenianie. A powstająca w niej stratyfikacja hamuje wentylację oceanu, czyli mieszanie powierzchniowych wód natlenionych z wodami głębszymi pelagicznymi i bentosowymi. A to z kolei prowadzi do odtleniania głębszych warstw oceanu. Ponadto, ludzie prowadząc działalność rolnictwa intensywnego doprowadzają często do tego, że ich nawozy azotanowe i fosforanowe stymulują rozwój bakterii i sinic, które w produkcji pierwotnej netto usuwają tlen z otoczenia wód morskich przybrzeżnych doprowadzając do ich odtleniania i wymierania wielu morskich gatunków przybrzeżnych.
W swoich wynikach badań, powyżej opisany zespół naukowy zauważył, że promieniowanie słoneczne ultrafioletowe oraz / lub podwyższona temperatura wyraźnie powodują zmniejszenie zwapnienia pośród glonów wapiennych. Natomiast u okrzemek został stwierdzony większy wzrost ich budowy krzemianowej przy podwyższonym poziomie CO2, ale i przy niewielkim nasłonecznieniu. Jednak zbyt intensywne światło słoneczne hamuje również rozwój tych glonów krzemianowych (Sunke Schmidtko i inni, 2017; Denise Breitburg i inni, 2018).
–
Refugia zakwaszenia oceanów
Zakwaszenie oceanów ma bardzo duży związek z wpływem na bioróżnorodność. Dwutlenek węgla, który w nadmiarze trafia do oceanów i mórz nie powoduje ich ogrzewania czy nawet odtleniania, ale jest częstą przyczyną ich zakwaszenia. Przede wszystkim mocno cierpi na tym fauna bezkręgowców morskich, które są zbudowane z wapiennych muszli i pancerzyków (np. małże i skorupiaki itp.).
Lydia Kapsenberg & Tyler Cyronak dokonali analizy przeglądowej tzw. refugiów zakwaszenia oceanów (OAR – Ocean Acidification Refugium), czyli obszarów morskich, w których gatunki ryb i bezkręgowców są w dużym stopniu narażone na wahania pH wód oceanicznych ze względu na zmienność w skali przestrzenno-czasowej strumienia dwutlenku węgla rozpuszczanego w nich 1.
Autorzy na wstępie pracy piszą:
Ostoje zmiany klimatu w lądowej biosferze to obszary, na których gatunki są chronione przed globalną zmianą środowiska i powstają w wyniku naturalnej różnorodności krajobrazów i klimatu. W obszarze morskim zakwaszenie oceanów lub globalny spadek pH wody morskiej pozostaje wszechobecnym zagrożeniem dla organizmów i ekosystemów. Naturalna zmienność chemii dwutlenku węgla (CO2) w wodzie morskiej stanowi jednak okazję do zidentyfikowania ostoi zakwaszenia oceanów (OAR) dla gatunków morskich.
Globalne pH powierzchni oceanów naturalnie waha się między pH 8,0 a 8,2 (Bates i inni, 2014) i przewiduje się, że spadnie o > 0,4 jednostki, jeśli emisje CO2 utrzymają się w obecnym tempie (Hans Otto Pörtner i inni, 2014).
Występuje wiele czynników biogeochemicznych i fizycznych, które mają dość potencjalnie duży wpływ na dynamikę lokalnego składu chemicznego dwutlenku węgla w wodzie morskiej i mogą one również podlegać takim samym dynamicznym zmianom parametrów fizycznych, jak np. temperatura, opady czy upwelling w systemie klimatycznym Ziemi.
–

Rys.1. Procesy modyfikujące ekspozycję na zakwaszenie oceanów w zakresie częstotliwości czasowych i skal przestrzennych. Źródło: Lydia Kapsenberg & Tyler Cyronak, 2019/CC BY 4.0.
—
Na panelu (a) ukazane są sezonowe reżimy pH napędzane przez ocieplenie w ekosystemie umiarkowanym i produkcję pierwotną w ekosystemie polarnym (Lydia Kapsenberg, Samir Alliouane i inni, 2017 ; Lydia Kapsenberg i inni, 2015). Na panelu (b) pokazana została zmienność pH w skali zdarzeń w okresie 5 tygodni. Produkcja pierwotna przez zakwit fitoplanktonu zwiększa pH, które zmniejsza się po zaprzestaniu zakwitu, podczas gdy okresowe zjawiska upwellingu powodują silne spadki pH (Lydia Kapsenberg, 2015 ; Lydia Kapsenberg & Gretchen E. Hofmann, 2016). Z kolei na panelu (c) przedstawione intensywne wahania pH w ekosystemie rafy koralowej są napędzane fotosyntezą bentosową i oddychaniem (Tyler Cyronak, Izaak C. Santos i inni, 2014).
Obszary refugiów zakwaszenia oceanu (OAR – Ocean Acidification Refugues), to przede wszystkim siedliska przybrzeżne jak namorzyny, trawy morskie, miejsca o wolnym przepływie wód, miejsca z daleka od upwellingu (wypływu wód bogatych w składniki pokarmowe dla zwierząt morskich), wzniesienia głębinowe itp.
–
Szybowiec Slocum mierzy pH oceanu
Pod względem ekonomicznym, duży ekosystem morski północno-wschodniego szelfu (NES – Northeast Shelf) Stanów Zjednoczonych obsługuje niektóre z najbardziej wartościowych łowisk przybrzeżnych w kraju. Jednak większość tych dochodów pochodzi z połowu skorupiaków, które są wrażliwe na zakwaszenie oceanów (OA – Ocean Acidification), którego prognozy wskazują w najbliższych latach na dalszy wzrost.
Grace Saba i Liza Wright-Fairbanks z Rutgers w Stanowym Uniwersytecie New Jersey oraz Baoshan Chen z Uniwersytetu Stony Brook i Wei-Jun Cai z Uniwersytetu Delaware w 2018 roku przetestowali szybowiec autonomiczny Slocum w kształcie żółtej torpedy, który przez trzy tygodnie mierzył pH, zasolenie i temperaturę wód oceanicznych w całym słupie wody przybrzeżnego Atlantyku, od portowego miasta Atlantic City do skraju podwodnego szelfu kontynentalnego na odcinku 130 mil, tam i z powrotem 1.
–

Fot. Szybowiec Slocum obsługiwany przez Rutgers University jest rozmieszczony u wybrzeży New Jersey. Podwodne szybowce wyposażone w czujniki dostarczają danych na żywo, które pomagają naukowcom zrozumieć w czasie rzeczywistym, jak zmienia się kwasowość w oceanach Ziemi. Źródło: Liza Wright-Fairbanks, Rutgers University/CC BY 4.0
–
Dane porównawcze pH mierzonego na północno-wschodnim szelfie kontynentalnym na różnych jego głębokościach, od powierzchni oceanu do dna, tradycyjną metodą spektrofotometryczną za pomocą pobierania próbek wody, a metodą za pomocą przemieszczania się automatycznego szybowca, wyraźnie się różniły. Okazało się, że pomiary czujnika pH z szybowca miały znacznie wyższą rozdzielczość z dokładnością 0,011 jednostek lub nawet lepszą, mierzoną non stop w ciągu kilku tygodni w całym słupie wody oceanicznej.
–
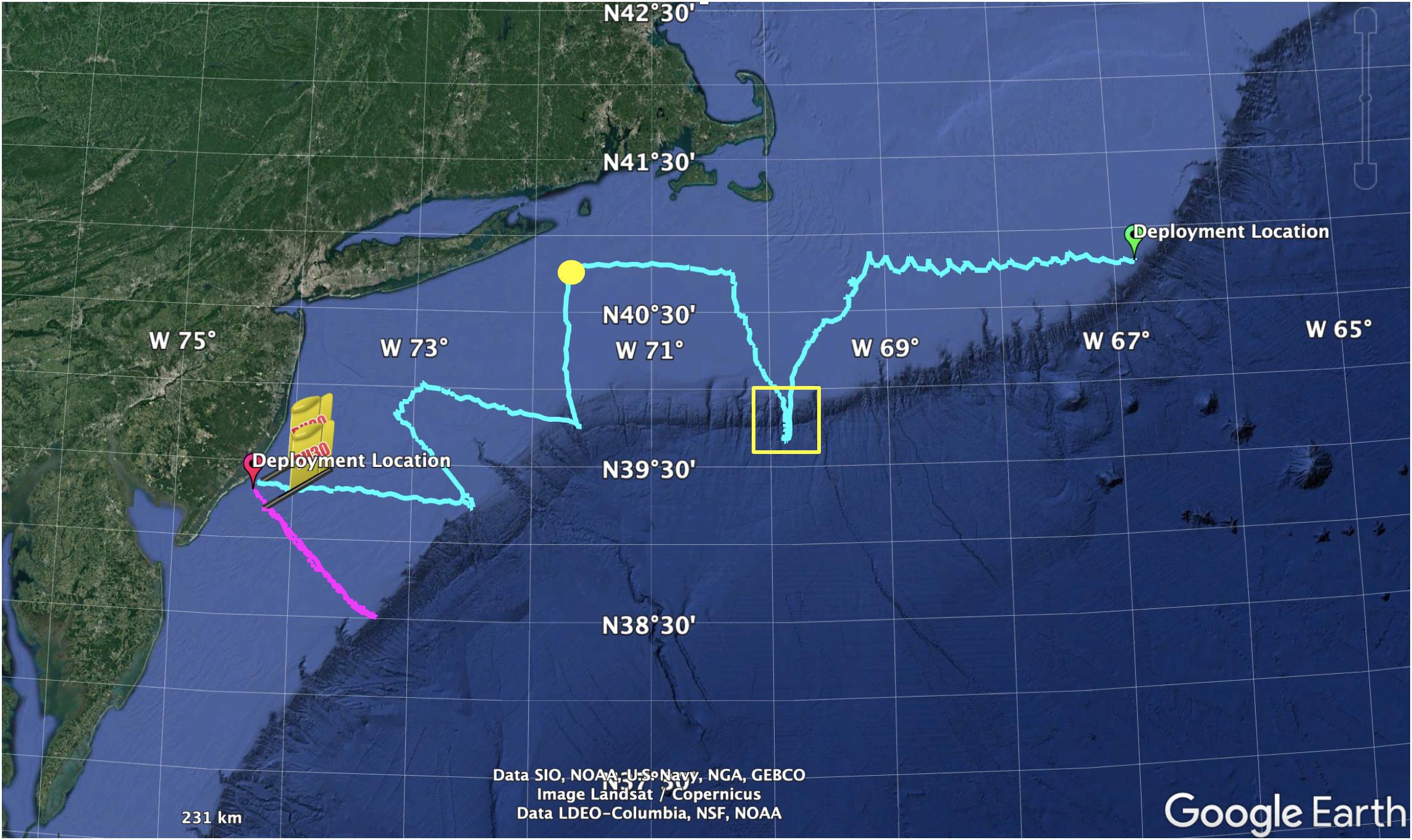
Rys. Mapa pokazująca lokalizację pierwszych wodowań szybowca pH. Źródło: Grace Saba & Liza Wrighr-Fairbanks, 2018/CC BY 4.0
–
Wodowania szybowca
W przypadku pierwszego wodowania (tor w kolorze magenta) szybowiec został zwodowany u wybrzeży Atlantic City w stanie New Jersey w dniu 2 maja 2018 r. i wykonał pomiary pH i innych zmiennych od przybrzeżnego do skraju szelfu kontynentalnego i z powrotem, gdzie został zacumowany 22 maja 2018 r.
W przypadku drugiego zwodowania (trasa w kolorze błękitnym), szybowiec został zwodowany na wschód od Georges Bank 5 lipca 2018 roku i wykonał pomiary pH i innych zmiennych podczas przepływu, dopóki nie został zacumowany u wybrzeży Atlantic City 28 sierpnia 2018 r. Podczas tego zwodowania szybowiec był wciągnięty w ciepły wir na prawie 5 dni (żółte równoległoboki i koło). Zaniepokojeni biodegradacją z powodu długiego okresu przebywania w ciepłej wodzie, 31 lipca szybowiec ten został przechwycony na południe od Montauk w stanie New Jersey w Stanach Zjednoczonych.
Ogólnie naukowcy ci zaobserwowali, że wcześniejsze wysiłki w zakresie monitorowania zakwaszenia miały albo zbyt niską rozdzielczość przestrzenną (cumowanie), albo z kolei zbyt wysokie koszty i zbyt niską rozdzielczość czasową oraz przestrzenną (rejsy badawcze).
W serwisie naukowym NOAA OAP (NOAA Ocean Acidification Program) prof. Grace Saba napisała 2:
Ten projekt optymalizuje sieć obserwacyjną NES OA obejmującą regiony środkowego Atlantyku i Zatoki Maine poprzez dodanie sezonowych rozmieszczeń podwodnych szybowców wyposażonych w transformujące, nowo opracowane i przetestowane głębokie czujniki pH oparte na ISFET oraz dodatkowe czujniki (pomiar temperatury, zasolenia dla całkowitej zasadowości i oszacowanie nasycenia aragonitem [ΩArag], tlenu i chlorofilu), optymalizacja istniejących regionalnych próbek w celu usprawnienia pomiarów chemii węglanów w kilku kluczowych lokalizacjach oraz kompilacja i integracja istniejących zasobów OA. Naukowcy zastosują te dane do istniejącego modelu ekosystemu/biogeochemii oceanicznej NES (BGC), który rozwiązuje chemię węglanów i jej zmienność.
–
Koralporoza – choroba koralowców
W 2020 roku naukowcy z Uniwersytetu w Edynburgu we współpracy z naukowcami z Uniwersytetu Heriot-Watt i Narodowej Administracji Oceaniczno-Atmosferycznej (NOAA – National Oceanic and Atmospheric Administration), badając głębinowe rafy koralowe w Pacyfiku u wybrzeży południowej Kalifornii zaobserwowali najniższy poziom pH na strukturach raf koralowych w historii pomiarów. Badaniami tymi kierował Sebastian J. Hennige z Grupy Badawczej Zmiany Oceanów oraz ze Szkoły Nauk o Ziemi na Uniwersytecie w Edynburgu 2.
Zespół amerykańskich naukowców z NOAA podjął badania tamtejszego ekosystemu raf koralowych za pomocą pojazdów podwodnych i zaobserwował wśród osobników koralowców gatunku Lophelia pertusa porowatość ich struktur. Następnie pobrał próbki tych żywych zwierząt i przekazał je do laboratorium w Edynburgu dla brytyjskich specjalistów od inżynierii środowiska, którzy z kolei w swoich zademonstrowanych eksperymentach w ciągu jednego roku zauważyli szybkie osłabienie szkieletów i odkryli uderzające podobieństwo do osłabienia obserwowanego w ludzkich kościach w wyniku osteoporozy. Nową chorobę zidentyfikowaną u Lophelia pertusa nazwali koralporozą albo koralowicą.
–

Fot.1. Koralowiec Lophelia pertusa z chłodnych wód głębinowych w południowej części Zatoki Kalifornijskiej. Po lewej stronie kolonia składająca się ze zdrowych osobników (białe korony) i chorych osobników na koralporozę (brązowo-szare podwaliny). Po prawej stronie kolonia składająca się z samych zdrowych osobników, ale na odsłoniętej skale o niskiej złożoności siedlisk. Nad oboma zdjęciami jest ukazana podziałka stanu nasycenia aragonitem (Ω Arag ) wód morskich w Zatoce Kalifornijskiej w badanym regionie. Kadr z obrazów w (a, b) został wykonany wraz z materiałem ROV przedstawiającym lokalizacje z dalszymi szczegółami lokalizacji. Źródło: Sebastian J. Hennige eta al., 2020/CC BY 4.0
–
Ekosystemy raf koralowych kurczą się także w głębinach
Oba zespoły naukowe zaobserwowały, że zarówno w warunkach laboratoryjnych, jak i w środowisku morskim, niski poziom pH powoduje pękanie i rozpad osobników koralowców laboratoryjnych Lophelia pertusa. Z kolei nurkując w pojazdach podwodnych w tamtym rejonie, zaobserwowali, że ekosystem koralowców tamtejszych oraz wielu innych gatunków zależnych od głębinowych raf koralowych już się kurczy, a w przyszłości przy dalszej nadmiernej absorpcji dwutlenku węgla przez oceany, ten proces jeszcze bardziej się nasili.
Główny autor pracy dr Sebastian Hennige ze Szkoły Geonauk (School of GeoSciences) na Uniwersytecie w Edynburgu w serwisie Science Daily napisał następująco 3:
Badanie to podkreśla, że głównym zagrożeniem dla tych wspaniałych ekosystemów głębinowych jest osłabienie strukturalne spowodowane zakwaszeniem oceanów, napędzanym przez rosnące ilości wytwarzanego przez nas dwutlenku węgla. Rafy głębinowe istnieją poza naszym zasięgiem wzroku, z pewnością o nich nie zapominamy, a nasza praca podkreśla, w jaki sposób naukowcy z różnych dyscyplin i krajów mogą połączyć siły, aby stawić czoła globalnym wyzwaniom.
Z kolei współautor badania, dr Peter Etnoyer z Narodowego Centrum Nauk Wybrzeży Oceanu (NCOS – National Centres for Coastal Ocean Science) w NOAA, stwierdził:
Koralowce głębinowe rosnące w południowej Kalifornii są oknem na przyszły ocean. Region jest naturalnym laboratorium do badania skutków zakwaszenia oceanów.
Natomiast dr Uwe Wolfram z Uniwersytetu Heriot-Watt w Edynburgu powiedział:
Dzięki możliwości dostosowania strategii do raf koralowych, które są rutynowo stosowane do monitorowania osteoporozy i oceny ryzyka złamań kości, możemy dysponować potężnymi nieinwazyjnymi narzędziami do monitorowania tych delikatnych ekosystemów.
–
Ekosystemy z większą różnorodnością biologiczną są odporniejsze niż te z mniejszą
Również w tym samym roku została przedstawiona ciekawa praca przez zespół naukowy Eugenio Rastelli’ego z Wydziału Nauk o Środowisku i Naukach Przyrodniczych, Politechniki Marche w Ankonie we Włoszech. Ukazała ona interesujące informacje naukowe, w których stabilne ekosystemy ze zróżnicowaną bioróżnorodnością morską są znacznie odporniejsze na zakwaszenie oceanów niż ich bardziej uproszczone odpowiedniki 4.
Przeanalizowano te badania na wybranych gatunkach koralowców, gąbek i makroglonów oraz innych organizmów morskich, w których stwierdzono też mniejszy wpływ oportunistycznych wirusów bentosowych na twardym dnie gdzie się kształtują zdrowe ekosystemy raf koralowych.
–

Rys.2. Wpływ zakwaszenia na taksony dominujące. Odnotowano zmiany tempa wzrostu różnych taksonów koralowych (czerwonych koralowców, kalcyfikujących glonów, niekalcyfikujących glonów, epilitycznych gąbek, endolitycznych gąbek, kalcyfikujących gąbek) spowodowane zakwaszeniem. Tempo wzrostu wyraża się jako zmiany masy w przypadku koralowca czerwonego lub w pokryciu powierzchni w przypadku makroglonów i gąbek. Podawane są wartości średnie i odchylenie standardowe (SD – Standard Deviation). Gwiazdki wskazują na istotne różnice (p < 0,01) w zabiegu zakwaszonym w porównaniu z odpowiednią kontrolą. Źrodło: Eugenio Rastelli et al., 2020/CC BY 4.0.
–
Na wstępie niniejszej pracy Rastelli zauważył zaskakujący wynik pracy przeprowadzony eksperymentalnie w Morzu Śródziemnym, a ściślej w Morzu Liguryjskim. Mianowicie, jego zdaniem utrata różnorodności biologicznej pod wpływem zmian klimatu zagraża jednocześnie ekosystemom morskim. Stwierdził, że hipoteza, pod względem współzależności między różnorodnością biologiczną, stanowiącą naturalne zespoły wielogatunkowe, a funkcjonowaniem ekosystemów morskich, w związku z zakwaszeniem oceanu nie jest jeszcze dokładnie przetestowana.
Rastelli w swojej pracy napisał:
Tutaj, w warunkach kontrolowanych eksperymentalnie, zbadaliśmy wpływ zakwaszenia na kluczowe organizmy tworzące siedliska (w tym koralowce, gąbki i makroglony) oraz powiązane mikroby w zbiorowiskach o twardym dnie, charakteryzujących się różnymi poziomami bioróżnorodności.
Nasze wyniki wskazują, że przy wyższej bioróżnorodności wpływ zakwaszenia na kluczowe organizmy, w inny sposób bardzo wrażliwe, można zmniejszyć o 50 do > 90%, w zależności od gatunku. Tutaj pokazujemy, że taki pozytywny wpływ większej bioróżnorodności może być związany z wyższą dostępnością zasobów żywności i zdrowym związkiem mikroorganizm-gospodarz, ogólnym zwiększeniem odporności gospodarza na zakwaszenie, przy jednoczesnym przeciwstawieniu się szkodliwym oddziaływaniom mikroorganizmów oportunistycznych.
Biorąc pod uwagę scenariusze zmian klimatu przewidywane na przyszłość, dochodzimy do wniosku, że ochrona różnorodności biologicznej ekosystemów o twardym dnie ma fundamentalne znaczenie również dla łagodzenia skutków zakwaszenia oceanów.
Warto też dodać, że wody morskie, gdzie w mezokosmach, przeprowadzano badania eksperymentalne są dość mocno wysycone wapieniami: aragonitem i kalcytem. A większe zróżnicowanie gatunkowe wskazuje na wspomnianą większą odporność badanych ekosystemów, zarówno pod względem wpływu zakwaszenia oceanu, jak i oddziaływania wirusów bentosowych na faunę bentosową.
W badanym regionie, najliczniejsza jest rodzina Corallidae z najliczniejszym gatunkiem, koralowcem czerwonym Corallium rubrum, w którym coraz rzadziej występują zróżnicowane biocenotycznie ekosystemy, w których występują najliczniejsze rodziny gąbek z rodzin: Hymedesmiidae , Ancorinidae , Clathrinidae , Leucosoleniidae i Sycettidae , mszywiołów: Celleporidae , Smittinidae , Beanidae , Crisiidae i Schizoporellidae , makroglonów: Hildenbrandiaceae i Hapalidiaceae, parzydełkowców: Dendrophylliidae i Epizoanthidae oraz wieloszczetów: Serpuloidae.
Podsumowując wyniki tej pracy, można stwierdzić, że ekosystemy raf koralowych z dominującym koralowcem czerwonym Corallium rubrum, ale silnie zubożone w gatunki z wyżej wymienionych zwierząt są najbardziej narażone na zakwaszenie oceanu.
–
Stan Wielkiej Rafy Koralowej jest krytyczny
Naukowy zespół Katharina E. Fabricius z Australijskiego Instytutu Morskich Nauk (Australian Institute of Marine Science) w Townsville, w 2020 roku przebadał stan raf koralowych w pobliżu dwóch oceanograficznych stacji pomiarowych w obrębie Wielkiej Rafy Koralowej. Stacji GBRWIS na Heron Island i stacji NRSYON na Yongala, na których mierzy się źródła zmienności składu chemicznego węgla w długofalowym trendzie czasowym 5.
Badacze w swojej pracy naukowej piszą, że dane z subtropikalnego środkowego szelfu GBRWIS obejmowały 3-godzinne zapisy z instrumentów, a dane z tropikalnego wybrzeża NRSYON były miesięcznymi próbkami wody morskiej.
Dokładna analiza badań w dekadzie 2009-2019 mówi bardzo wyraźnie, że Wielka Rafa Koralowa już jest w dłuższej perspektywie czasu nie do uratowania.
Na obu stacjach zaobserwowano duże wahania lotności dwutlenku węgla (f CO2) w wodzie morskiej, na które nałożyły się wahania sezonowych i dziennych fluktuacji temperatury i zasolenia.
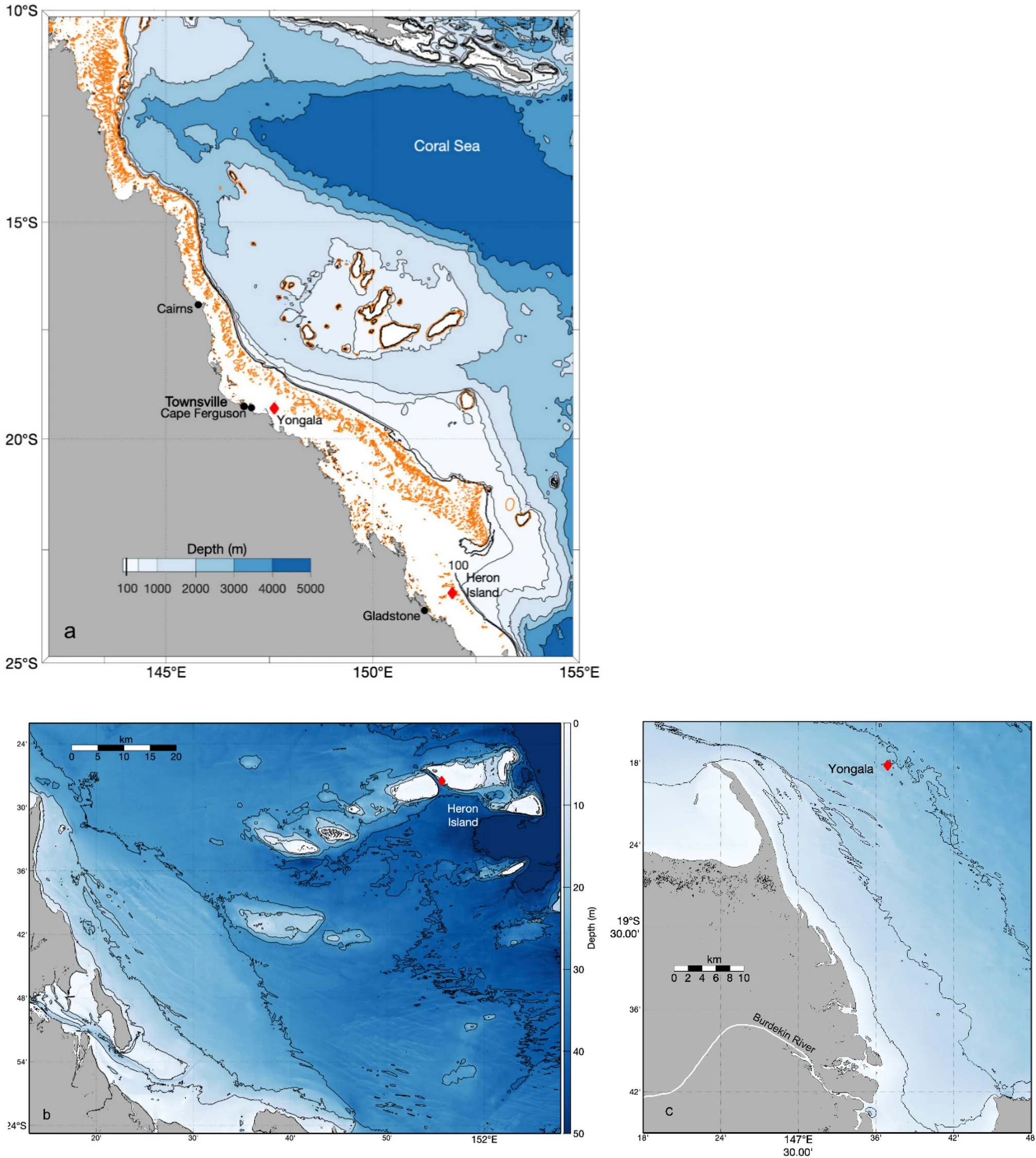
Rys.3. Mapa Wielkiej Rafy Koralowej (linie pomarańczowe: rafy koralowe) i stacji referencyjnej gazów atmosferycznych Cape Ferguson ( a ) oraz stacji oceanograficznych GBRWIS ( b ) i NRSYON ( c ). Niebieskie cieniowanie wskazuje na batymetrię, a gruba czarna linia przedstawia 100-metrową linię batymetrii. Liczby zostały wygenerowane przy użyciu danych batymetrycznych z 30-metrowego modelu głębokości dla Wielkiej Rafy Koralowej – RJ Beaman. Źródło: Pobrano zdjęcia z Geonauk Australii (Geoscience Australia) https://ecat.ga.gov.au/geonetwork/srv/eng/catalog.search#/metadata/115066 oraz wykreślono za pomocą oprogramowania Matlab w wersji R2020a z pakietem mapującym M_Map (wersja 1.4 m, autorstwa R. Pawlowicza, https://www.eoas.ubc.ca/~rich/map.html).
–
W ciągu zbadanych 10 lat, lotność dwutlenku węgla (fCO2) na obu stacjach wzrosła o > 2,0 ± 0,3 µatm w ciągu roku. Również w tym samym czasie zaobserwowano wzrost temperatury i zasolenia wody morskiej, a także jej pH. Ponadto, stan nasycenia aragonitem spadł bardzo wyraźnie. I na to wygląda, że wszystkie te wymienione parametry będą dalej spadać, jeśli będziemy dalej w takiej ilości jak obecnie emitować dwutlenek węgla do atmosfery i do oceanów.
Autorzy tejże pracy piszą:
Dekadowy trend wzrostowy lotności (f) CO2 pozostał istotny w danych znormalizowanych dla temperatury i zasolenia. Rzeczywiście, roczne minima f CO2 są obecnie wyższe niż szacowane maksymalne wartości f CO2 na początku lat sześćdziesiątych XX wieku, czyli średnio, lotność CO2 teraz wynosi o 28% więcej niż 60 lat temu. Nasze dane wskazują, że rozpuszczanie węglanów z dna morskiego sprawia, że nie jesteśmy obecnie w stanie ochronić Wielkiej Rafy Koralowej przed zakwaszeniem oceanów. Ma to ogromnie niepokojące znaczenie dla tysięcy raf koralowych i innych różnorodnych ekosystemów morskich znajdujących się w tym rozległym systemie szelfu kontynentalnego.
–
Zakwaszenie oceanu powoduje zaburzenia słuchu u ryb
W latach 2021–2025 przeprowadzono istotne badania nad wpływem zakwaszenia oceanu na zdolności słuchowe ryb.
Jedno z kluczowych badań zostało opublikowane w 2021 roku przez zespół naukowców z Uniwersytetu Auckland w Nowej Zelandii: C. A. Radforda, S. P. Collins, Phila L. Mundaya i Darrena Parsonsa.
Badacze skupili się na młodych osobnikach ryby Chrysophrys auratus, hodowanych w warunkach przewidywanego przyszłego zakwaszenia oceanu (pCO₂ ≈ 1000 µatm). W tym celu do analizy wpływu podwyższonego poziomu CO₂ na słuch wspomnianego gatunku ryb zostały użyte techniki takie jak:
- potencjały wywołane słuchowo (AEP)
- mikrotomografia komputerowa (microCT) .
Wyniki wykazały znaczący spadek czułości słuchu w zakresie niskich częstotliwości (<200 Hz) u ryb, które były poddane wyższemu stężeniu CO₂. Skutki były takie, że u tych morskich zwierząt w uchu wewnętrznym nastąpiło asymetryczne powiększenie otolitów (kamieni słuchowych). Naukowcy przypuszczają, że mogło to doprowadzić je do obniżonej zdolności słyszenia.
Autorzy stwierdzili, że zakwaszenie oceanu mogło wpłynąć na słuch na dwa sposoby. Zarówno poprzez bezpośrednie oddziaływanie na narządy słuchowe, jak i poprzez zmiany w zachowaniach związanych ze słuchem. To badanie stanowi pierwsze empiryczne powiązanie przewidywanych przyszłych warunków w wodzie oceanicznej z podwyższonym stężeniem CO₂ z modyfikacjami anatomii słuchowej i obniżenia jakości zdolności słuchowych ryb.
Badacze nowozelandzcy i australijscy w swojej pracy piszą:
Dźwięk podwodny jest skutecznym kanałem sensorycznym, ponieważ jest wielokierunkowy i może przenosić ważne informacje o lokalizacji i jakości siedlisk oraz innych zwierząt [ 17 – 20 ]. Słuch odgrywa kluczową rolę w strategiach życiowych ryb, w tym w orientacji i reakcji osiedlania się larw ryb [ 21 – 24 ], synchronizacji tarła [ 25 , 26 ], zalotach i wyborze partnera [ 27 , 28 ] oraz wołaniu kontaktowym [ 29 ]
–
Otolity
Tutaj naukowcy zwrócili uwagę na wrażliwość wapiennych składników w uszach ryb, mianowicie otolitów:
Otolity składają się z aragonitu [ 33 , 34 ] i początkowo uważano, że wapnienie otolitów może być upośledzone w zakwaszonych warunkach ze względu na zmniejszone nasycenie węglanem w wodzie morskiej o niskim pH [ 35 ]. Jednak spójnym odkryciem w badaniach nad zakwaszeniem oceanów u ryb jest to, że otolity są często większe u larw ryb narażonych na podwyższone warunki CO2 [ 33 , 36–40 ] .
W tym badaniu eksperci wykorzystali technikę elektrofizjologiczną, czyli potencjały wywołane słuchowo (AEP), w taki sposób aby bezpośrednio przetestować wpływ warunków zakwaszenia oceanu na zdolność słyszenia larw Chrysophrys auratus. We wcześniejszych badaniach potencjały te miały szerokie zastosowanie do pomiaru progów słuchowych ssaków [ 57 ]. Obecnie zostały zaadaptowane do pracy nad rybami [ 58 , 59 ].
Przyszłość jest taka, jeśli dalej będzie trwało globalne ocieplenie atmosfery i wód oceanicznych na świecie, to najprawdopodobniej rybom będzie pogarszać się słuch w zakwaszonej wodzie o coraz niższym pH, o czym przestrzegają badacze z Nowej Zelandii i Australii. Niewykluczone, że ten problem laryngologiczny może dotykać inne grupy zwierząt morskich, w tym ssaków i ptaków nurkujących.
–
Obszerna metaanaliza kalcyfikatorów
Jonathan Y.S. Leung, Sam Zhang i Sean D. Connell z Uniwersytetu w Adelaide zaprezentowali systematyczny przegląd i metaanalizę, które obejmowały 985 badań z ostatnich dwóch dekad, obejmujących łącznie 5153 obserwacje, i miała na celu ponowną ocenę wpływu zakwaszenia oceanu na organizmy wapniejące (kalcyfikujące).
Naukowcy z Australii zbadali, iż wiele organizmów morskich wykazuje zróżnicowaną wrażliwość taksonomiczną. Ich zdaniem, do końca XXI wieku organizmy takie jak jeżowce, skorupiaki i głowonogi posiadają tolerancję poziomu zakwaszenia pH ≈ 7,8. Natomiast kokolitofory, glony wapniejące i koralowce są niestety bardziej wrażliwe na zmiany pH.
–

Fot. Komórki Coccolithophore pokryte łuskami węglanu wapnia (kredy). Postęp w zrozumieniu unikalnej fizjologii tych globalnie ważnych organizmów pomoże nam zrozumieć, jak mogą one reagować na zmieniającą się chemię oceanów. Źródło: Robin Mejia. Zdjęcie dzięki uprzejmości dr Alison Taylor/CC BY-SA 4.0
–
Negatywny wpływ spadku pH w wodzie oceanicznej na stadia larwalne niż na dorosłe u kalcyfikatorów
W etapie rozwojowym larwalne stadia organizmów wapniejących (kalcyfikatorów) są generalnie bardziej podatne na zakwaszenie niż formy dorosłe. Dobra wiadomość jest taka, iż ponad 70 proc. obserwacji dotyczących wzrostu i wapnienia nie wykazało negatywnych efektów, co sugeruje, że wiele organizmów posiada zdolność do aklimatyzacji poprzez:
-
-
plastykę fenotypową (zmiany fizjologiczne, mineralogiczne, strukturalne i molekularne),
-
plastykę transgeneracyjną,
-
zwiększoną dostępność pokarmu,
-
interakcje międzygatunkowe.
-
Badanie te wyraźnie sugeruje w optymistyczny sposób, że wpływ zakwaszenia oceanu na organizmy wapniejące może być mimo wszystko mniej szkodliwy niż wcześniej sądzono. Głównie ze względu na niedocenianą zdolność adaptacyjną tych organizmów do zmiennych warunków środowiskowych, w tym pH wody morskiej. Autorzy podkreślają, ze przyszłe badania powinny być też skoncentrowane na pozytywnych skutkach, a nie tylko negatywnych. A więc przede wszystkim na mechanizmach przetrwania i adaptacji organizmów morskich w zmieniających się warunkach środowiskowych w coraz cieplejszym świecie.
Naukowcy w swojej publikacji naukowej stwierdzili:
Przewiduje się, że oceany będą w przyszłości zakwaszane w niespotykanym dotąd tempie, naukowcy zajmujący się oceanami wyrażają poważne obawy dotyczące potencjalnego wpływu zakwaszenia oceanów na organizmy morskie. Osoby budujące struktury wapienne (tj. morskie kalcyfikatory) są uważane za szczególnie podatne, ponieważ oczekuje się, że wapnienie będzie utrudnione przez zmniejszoną wartość Ω wody morskiej. [ 6 ] Ponadto zakwaszona woda morska jest uważana za „żrącą” i może powodować rozpuszczanie minerałów CaCO3 . [ 24 ] W konsekwencji wapnienie netto (tj. wapnienie brutto minus rozpuszczanie brutto) zmniejsza się, a struktury wapienne stają się bardziej kruche. Oprócz upośledzonego wapnienia, zakwaszenie oceanów może również wywołać kwasicę (tj. zwiększoną kwasowość płynów ustrojowych), która może osłabić wiele ważnych procesów fizjologicznych, takich jak metabolizm tlenowy. [ 25 ] Depresja metaboliczna z kolei opóźnia produkcję energii, która wspomaga wapnienie i wiele innych procesów i aktywności biologicznych. Chociaż kwasicę wywołaną CO2 można zrekompensować poprzez regulację kwasowo-zasadową, do aktywacji powiązanych transporterów i wymienników jonów wymagana jest energia [ 25 ] , co sugeruje kompromis energetyczny na rzecz kalcyfikacji. Krótko mówiąc, obniżona wartość Ω wody morskiej, nasilone rozpuszczanie CaCO3 i zaburzona fizjologia są uważane za główne czynniki ograniczające zdolność kalcyfikatorów do budowania struktur wapiennych w warunkach zakwaszenia oceanów.
–
Referencje:
- Feely R. et al., 2006 ; Carbon Dioxide and Our Ocean Legacy ; Smithsonian Institution ; https://www.pmel.noaa.gov/pubs/PDF/feel2899/feel2899.pdf
- Bennett J., 2006 ; Ocean Acidification ; Smithsonian ; https://ocean.si.edu/ocean-life/invertebrates/ocean-acidification
- Riebesell U. et al., 2016 ; Competitive fitness of a predominant pelagic calcifier impaired by ocean acidification ; Nature Geoscience ; https://www.nature.com/articles/ngeo2854
- Gao K. et al., 2019 ; Effects of Ocean Acidification on Marine Photosynthetic Organisms Under the Concurrent Influences of Warming, UV Radiation, and Deoxygenation ; Global Change and the Future Ocean ; https://www.frontiersin.org/articles/10.3389/fmars.2019.00322/full
-
Kapsenberg L. et al., 2019 ; Ocean acidification refugia in variable environments ; Global Change Biology ; https://onlinelibrary.wiley.com/doi/full/10.1111/gcb.14730
- Saba G. K. et al., 2018 ; The Development and Validation of a Profiling Glider Deep ISFET-Based pH Sensor for High Resolution Observations of Coastal and Ocean Acidification ; Observation Ocean ; https://www.frontiersin.org/articles/10.3389/fmars.2019.00664/full
- Saba G. K., 2020 ; OAP Projects in the Southeast U.S. Optimizing Ocean Acidification Observations for Model Parameterization in the Coupled Slope Water System of the U.S. Northeast Large Marine Ecosystem ; NOAA OAP ; https://oceanacidification.noaa.gov/CurrentProjects/Southeast/TabId/2910/ArtMID/14230/ArticleID/15729/Optimizing-Ocean-Acidification-Observations-for-Model-Parameterization-in-the-Coupled-Slope-Water-System-of-the-US-Northeast-Large-Marine-Ecosystem.aspx
-
Hennige S. J. et al., 2020 ; Crumbling Reefs and Cold-Water Coral Habitat Loss in a Future Ocean: Evidence of “Coralporosis ; Deep-Sea Environments and Ecology ; https://www.frontiersin.org/…/10…/fmars.2020.00668/full
-
University of Edinburgh, 2020 ; Ocean acidification puts deep-sea coral reefs at risk of collapse ; Science Daily ; https://www.sciencedaily.com/rel…/2020/09/200917105321.htm
-
Rastelli E. et al., 2020 ; A high biodiversity mitigates the impact of ocean acidification on hard-bottom ecosystems ; Scientific Reports ; https://www.nature.com/articles/s41598-020-59886-4
-
Fabricius K. E. et al., 2020 ; Progressive seawater acidification on the Great Barrier Reef continental shelf ; Scientific Reports ; https://www.nature.com/articles/s41598-020-75293-1
- Radford C. A. et al., 2021 ; Ocean acidification effects on fish hearing ; Biological Sciences ; https://royalsocietypublishing.org/doi/full/10.1098/rspb.2020.2754
- Leyng J. Y. S. et al., 2022 ; Is Ocean Acidification Really a Threat to Marine Calcifiers? A Systematic Review and Meta-Analysis of 980+ Studies Spanning Two decades ; NANO-MICRO small ; https://onlinelibrary.wiley.com/doi/10.1002/smll.202107407
